推荐产品
公司新闻/正文
qPCR结果都不一样?这些技巧你需要掌握!
人阅读 发布时间:2023-10-27 10:21
简介
实时荧光定量PCR(Quantitative Real-time PCR)也称 QPCR,是指在DNA 扩增应中,以荧光化学物质测单次聚合酶链式反应(PCR)循环后产物总量的方法。
原理与操作
QPCR 技术实现了 PCR 从定性到定量的飞跃,以特异性强、重复性好、定量准确、可实时监测等优点成为了分子生子生物学研究中常用工具。
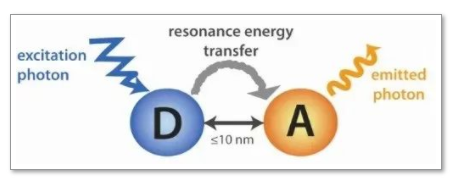
QPCR 自1983年发明以来,经过数次更新迭代,到如今在实验中广泛运用,
做过qPCR(荧光定量PCR)的小伙伴,可能会遇到这样的问题,明明已经按照文献的方法,照搬PCR引物,可还是每次结果都不一样。
其实原因有这么几个:
一、操作原因,你可能不太会用移液枪
有些小伙伴可能会说,移液枪使用多么简单,怎么可能不会用?实际上,在使用移液枪,特别是微量移液枪的时候,我们往往会长期快速操作,也就是说在弹簧还没来得及恢复的时候,我们已经又按了一下了。这样可能导致的结果不用我多说,首先可能会导致……指关节受伤。当然,这些只是其次,最重要的是会影响移液量。
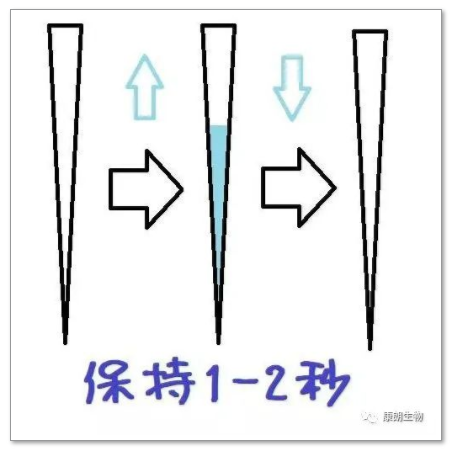
所以,关爱拇指,吸取液体时,保持1-2秒,给弹簧一个缓冲。当然,在加模板的时候,提高模板加样量,也可以尽可能减少每次加样的误差。
吸取液体的时候,需要把枪头插入凹液面底部,而不是插到凹液面的侧面。侧面比较容易产生气泡:
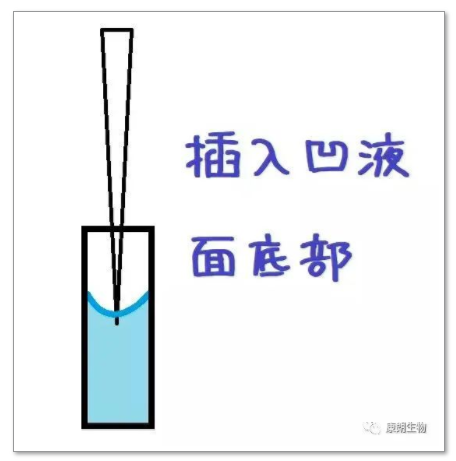
当然,你会说,每次枪头都插很深(莫名其妙觉得是在开车),但是这样的话,就很容易在枪头上沾上液滴,在微量的模板加样时,很容易导致加样量的误差。
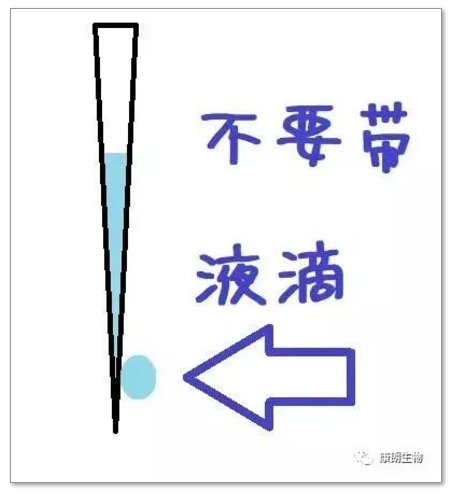
二、RNA的降解,也就是RNA完整性的问题
RNA的完整性,一般体现在电泳过程中18S和28S的亮度上,如果这两个条带的RNA亮度变低,甚至没有,就说明RNA的完整性应该会有损失。(但实际上现在没人去跑电泳)导致RNA完整性受损的原因有很多,比如:
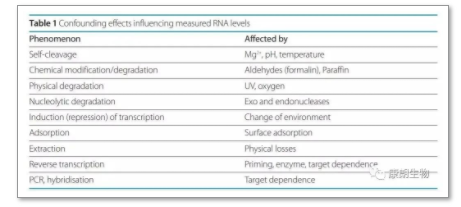
包括镁离子,pH,温度,紫外线,福尔马林等等都会对你的RNA产生影响。所以,要处处小心。于是有人做了这样的实验,就是对于RNA的降解,有没有什么方法可以降低RNA降解对于qPCR的影响。
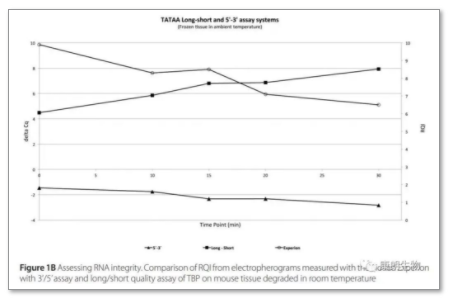
他们分别分析了3`端和5`端的扩增CT值,以及长片段和短片段的ΔCT,发现RNA的完整性缺失与3`端和5`端没多大关系,但是短片段会比长片段扩增效率更高。所以,qPCR引物设计的过程中,尽量把片段设计得短一点。
三、抑制物,这点相对难解决
在反转录过程中或者PCR过程中都可能有抑制物,这些抑制物,比如Na离子,EDTA,SDS,酚,血红素,腐植酸等等,都会对qPCR结果产生影响。具体体现在扩增曲线里会是这样:
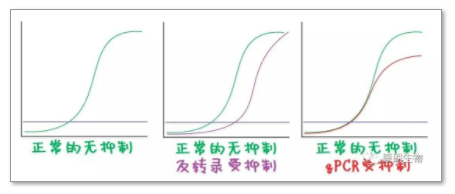
实际上去除抑制剂也只能在抽提的过程中尽量洗脱掉抑制剂,别的操作过程中其实也没什么办法(加促进剂可能又会产生不稳定因素)。
我们往往谨慎对待:引物、探针、Ct 值等,但也有一些小东西会被忽视,比如:ROX™。也许很多同学的第一反应是:总听人说起 ROX™,但它是什么?它在荧光定量 PCR 里起到什么作用呢?
其实和 FAM™、VIC™、SYBR™ Green 类似,ROX™ 也是一种在 qPCR 反应中能被 qPCR 仪检测到的荧光染料分子。但与其他染料不同,ROX™ 是一种惰性参比染料,也就是说,其荧光信号并不随着 PCR 扩增而增强。相反,ROX™ 的荧光信号值在反应中是基本保持不变的。
四、ROXTM 有什么问呢?
其实,在 qPCR 反应中有许多反应本身的物理因素会影响信号检测,从而造成孔间数据的差异。例如:PCR 反应板本底信号不均一,PCR 管盖厚度有差异,同一反应体系在分装时出现了差异等因素。ROX™ 能帮助我们通过均一化校正消除这些因素的误差,从而提高数据精确性。